-
![[image]](https://www.balancer.ru/cache/sites/com/sp/sputnikvaccine/local/templates/sputnik/img/infographics/128x128-crop/rus.png)
Вакцины и вакцинирования - только медико-биологические аспекты
Биология, экономика, логистика и т.п. вакцинТеги:
Только я про Ходжу подумал?

Мурашко добавил, что результаты клинических исследования «КовиВака» и «ЭпиВакКороны» будут опубликованы в конце 2021 года либо в первом квартале 2022 года.

Мурашко назвал сроки публикации данных об исследовании российских вакцин
Результаты клинических исследований российской вакцины от коронавируса Спутник V будут представлены к октябрю, данные по остальным вакцинам к концу этого началу следующего года. Об этом заявил ... // www.rbc.ru

Invar> Только я про Ходжу подумал?
Это ж совсем не то же самое, что результаты за бугром.
Опять ива в бан- инвар отдувается, создавая видимость войнушки клуба отстойных?
Это ж совсем не то же самое, что результаты за бугром.
Опять ива в бан- инвар отдувается, создавая видимость войнушки клуба отстойных?


Fakir:
предупреждение (+1) по категории «Флуд или офтопик»
- Fakir [30.07.2021 22:27]: Предупреждение пользователю: Bredonosec#28.07.21 13:46
Известия 

 про "ЭпиВакКорону" 3К:
про "ЭпиВакКорону" 3К:
Про заболевших - ничего. Про IgM и ПЦР


...



 про "ЭпиВакКорону" 3К:
про "ЭпиВакКорону" 3К:На 42-й день после вакцинации «ЭпиВакКороной» антитела IgG к коронавирусу были найдены у 79% привитых добровольцев и 11,6% человек из группы плацебо. Эти промежуточные результаты отражены в обзоре контроля качества третьей фазы клинических испытаний вакцины, с которым ознакомились «Известия». На основании полученных данных сделаны выводы об эффективности «ЭпиВакКороны». 79% — это иммунологическая, а не эпидемиологическая эффективность
Про заболевших - ничего. Про IgM и ПЦР



С каждым добровольцем провели девять встреч (так называемых визитов исследования) для наблюдения за их состоянием и отбора проб. Особенно важными были встречи № 1, когда провели первичную вакцинацию, № 5, когда сделали вторую прививку, и № 9 — на 42-е сутки, когда должны выработаться антитела к коронавирусу.
...
Также специалисты КРЛаб получили данные по антителам IgM, которые вырабатываются во время активного COVID-19. По этому показателю на визите № 5 не было найдено статистически значимых различий между исследуемыми группами: IgM не обнаружен у 96,9% добровольцев из основной группы и у 95,3% добровольцев из группы сравнения. Похожие результаты получены и на встрече № 9. Это говорит о том, что «ЭпиВакКорона» никого не инфицирует.
Эти данные были подтверждены тестами ПЦР, которые также провели на пятой и девятой встречах. РНК SARS-CoV-2 не обнаружена у 95,7% добровольцев из основной группы и у 94,1% человек из группы сравнения. На визите № 9 — у 99,4% из числа привитых и у 98,9% получивших плацебо.

Войти в контроль: обнародованы промежуточные итоги испытаний «ЭпиВакКороны»
Иммунологическая эффективность препарата — 79%, у стольких привитых найдены антитела // iz.ru


Ученые сравнили эффективность разных вакцин против штамма "дельта"
Известные вакцины долгое время подтверждали высокую эффективность против коронавируса, но из-за дельта-штамма показатели стали снижаться // lv.sputniknews.ru

Эффективность "Спутника V" против дельта-штамма составляет 83%, рассказали в Минздраве. Это самый высокий показатель среди вакцин. Moderna показала защиту в 76%, а Pfizer — всего 42%. Результаты исследования разместили на сайте MedRxiv. В нем участвовали 180 тысяч человек pic.twitter.com/ElgQZD76vl
— РИА Новости (@rianru) August 12, 2021
Эффективность "Спутника V" против дельта-штамма составляет 83%, рассказали в Минздраве. Это самый высокий показатель среди вакцин. Moderna показала защиту в 76%, а Pfizer — всего 42%. Результаты исследования разместили на сайте MedRxiv. В нем участвовали 180 тысяч человек.

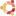
О ревакцинации:
Заголовок, конечно, из разряда изнасилование журналиста:

вот тут интереснее:

Заголовок, конечно, из разряда изнасилование журналиста:

Lancet опубликовал данные о бесполезности массовой ревакцинации от COVID
Группа ученых, среди которых руководители ВОЗ, заявили, что если пациентам вводить бустерные дозы вакцин слишком рано или слишком часто, то это может вызвать миокардит или синдром Гийена-Барре // www.rbc.ruвот тут интереснее:

Споры о ревакцинации против COVID-19
Тема ревакцинации против COVID-19 в последние дни заняла центральной место в англоязычных СМИ. Триггером послужила публикация в Lancet под рубрикой «Точка зрения» (Viewpoint) статьи, авторы которой выступают против массовой ревакцинации (… // prof-afv.livejournal.comВОЗ акцентирует гуманитарно-гуманистический аспект - дилемма ревакцинировать ли «избранных» или вакцинировать «обделённых», когда вакцины на то и другое недостаточно. Статья же освещает проблему с иного ракурса.
В ней акцент перенесен на анализ того, какие условия должны быть выполнены для принятия решения – начинать ревакцинацию или нет. Авторы считают, что такое решение должно приниматься только при наличии соответствующей доказательной базы. В общем виде, с этим трудно спорить.
Но авторы не ограничиваются общими словами, а приводят конкретные научные данные, свидетельствующие о том, что необходимости в массовой ревакцинации сейчас нет.
Оговорюсь, большая часть этих данных, получена при использовании «западных» вакцин против COVID-19. Прежде всего это PfizerBioNTech, Moderna (мРНК вакцины) и AstraZeneca (аденовирусная-векторная), в меньшей степени Johnson& Johnson (аденовирусная-векторная) и, совсем в малой степени, Novavax (субъединичная). В анализ вошли и данные о протективности китайских инактивированных вакцин. В отношении Спутника ясности нет. В тексте статьи он не упоминается. Но не исключено, что данные по Спутнику включены в группу аденовирусные-векторные.
Итак, в «сухом остатке»:
· протективность против тяжёлого COVID-19 уменьшилась незначительно.
· общая протективность уменьшилась сильнее, но остаётся выше 80%. Даже у «аутсайдеров» (инактивированных вакцин) протективность остаётся высокой – выше 80% против тяжелого COVID-19 и выше 60% против инфицирования и заболевания.
· «проблемные варианты» (VOC), конечно, проблемы создают, но даже в самом зловредном случае (гамма) протективность против тяжелого COVID-19 близка к 80% и выше 60% против инфицирования и заболевания.
Из этого, по мнению авторов, следует, что сейчас нет необходимости в массовой «всеобщей» ревакцинации тех, кто привит вакцинами, вошедшими в их анализ. Посмотрим, согласится ли с ними FDA.
Что касается ревакцинации российскими вакцинами, то подобный анализ невозможен из-за отсутствия необходимых данных.


В Эстонии коронавирусом чаще всего заражаются люди, вакцинированные препаратом AstraZeneca, сообщает портал ERR.


В Эстонии назвали вакцину, после которой COVID-19 заражаются чаще всего
Считать одну вакцину лучше других в условиях меняющихся данных нецелесообразно, заявили в республике // lt.sputniknews.ru


CDC: Moderna защищает от госпитализации лучше других СOVID-вакцин
Исследование Центров по контролю и профилактике заболеваний (CDC) США показало, что препарат компании Moderna является наиболее эффективным от госпитализации при COVID среди других вакцин, хотя вакцины Pfizer и Johnson & Johnson также обеспечивают существенную защиту. Об этом сообщает РБК-Украина со ссылкой на The Hill. // bb.lv

Вакцина Pfizer способствует появлению рака?
Растет также количество онкологических заболеваний. Об этом сообщает издание World Net Daily со ссылкой на статистические данные, а также на информацию доктора Райана Коу, сертифицированного паталогоанатома, владельца и директора диагностической лаборатории.
По словам Коу, с начала 2021 года он наблюдает в лаборатории 20-кратное увеличение случаев рака эндометрия (злокачественная опухоль, развивающаяся из эпителиальных клеток слизистой оболочки матки). Врач также предупредил об «огромном всплеске» различных аутоиммунных заболеваний (вызваны сбоями в работе иммунитета) и рака у пациентов, получивших прививки.

Растет также количество онкологических заболеваний. Об этом сообщает издание World Net Daily со ссылкой на статистические данные, а также на информацию доктора Райана Коу, сертифицированного паталогоанатома, владельца и директора диагностической лаборатории.
По словам Коу, с начала 2021 года он наблюдает в лаборатории 20-кратное увеличение случаев рака эндометрия (злокачественная опухоль, развивающаяся из эпителиальных клеток слизистой оболочки матки). Врач также предупредил об «огромном всплеске» различных аутоиммунных заболеваний (вызваны сбоями в работе иммунитета) и рака у пациентов, получивших прививки.

Американский врач: заболеваемость раком у вакцинированных пациентов увеличилась в 20 раз
Американская федеральная система отчетности о нежелательных последствиях после вакцинации от короновируса столкнулась с масштабным увеличением числа проблем. Растет также количество онкологических заболеваний. // u-f.ru


В Израиле окончательно поняли, нужна ли третья прививка от Covid-19
"Появились первые результаты расширенной израильской программы вакцинации - и они свидетельствуют о заслуживающем внимания эффекте ревакцинации. Израильские ученые под руководством Йинона Бар-Она проанализировали данные в общей сложности 1,1 млн человек в своей стране, все из которых были не моложе 60 лет и уже были полностью привиты вакциной компании Biontech; часть из них также была ревакцинирована тем же препаратом", - пишет немецкое издание Süddeutsche Zeitung. Перевод - InoPressa. // bb.lv

Интервью с чумаковцами от 28 июня

...
Когда мы занимаемся разработкой вакцин, то пытаемся сделать эффективный и безопасный препарат — без оглядки на то, что сделали наши коллеги. Более того, мы полагаем, что в результате, когда пройдет какое-то время, возможно, самым оптимальным вариантом будет использовать разные модальности для ревакцинации.
На мой взгляд, вопрос о конкурентной бизнес-модели, о том, что мы будем продавать нашу вакцину с такими-то параметрами, а значит, «Спутник» себя будет продавать вот таким образом, некорректен. Мы это не для денег делаем.
...
Козловская: Мы не знаем, что будет через полгода. Мы, например, не знаем, кому нужны ревакцинации, сколько их будет нужно. И вообще, можно ли считать людей, привитых год назад, привитыми до сих пор. Нам предстоит собрать еще миллионы эпидемиологических данных. И в какой-то момент каждая из вакцин либо займет собственную нишу и будет существовать в ней — получит преимущества для людей каких-то определенных категорий, для каких-то определенных ситуаций и так далее, — либо обе вакцины будут взаимозаменяемыми.
...
— А сколько уже людей участвуют в исследованиях третьей фазы?
Синюгина: Исследования еще не начаты. У нас сейчас одобрено 18 клинических баз [лечебных учреждений], на три клинические базы мы ждем одобрения. Как только получим, начнем набор добровольцев…
— И там, в клиническом исследовании, половина доз — это плацебо?
Синюгина: Нет. Это неэтично с точки зрения эпидемиологической ситуации в России. Поэтому это открытое исследование без плацебо.
— Как определяется протективная эффективность препарата в исследованиях без плацебо?
Козловская: На сравнении с идентичной группой непривитых людей их популяции.
Синюгина: Мы прекрасно понимаем, что сейчас проводить плацебо-контролируемые исследования такого объема неэтично.
— Расскажите про вторую фазу исследований — про иммуногенность. Какие результаты вы получили, когда будет по ним информация? И когда будет [научная] статья по итогам второй фазы?
Козловская: Статья по доклиническим исследованиям отправлена на рецензию в один из ведущих зарубежных журналов.
...
Кордубан: У нас прошла первая фаза [исследований] — безопасность. Мы доказали свою безопасность. Дальше у нас идет вторая фаза — иммуногенность. Она проходила поэтапно: 200 человек в одной части, еще 200 — в другой. Финальный отчет, обработанный статистиками, мы должны получить в конце недели.
— А в вашем штамме, конечно, уханьский вирус?
Козловская: Нет. У нас европейский вариант с мутацией, D614G.
— Это подводит меня к вопросу: эффективна ли ваша вакцина против штамма дельта?
Козловская: Если бы он у меня был, если бы мне его кто-нибудь подарил… Нам пришлось, как и в первый раз, выделять его от больных, а в это время…
— В Институте Гамалеи вакцину проверяли на этом штамме, но с вами не поделились?
Козловская: Нет. Мы сейчас проверяем нашу вакцину на штамм дельта по смывам, которые получаем из больниц.
— А вы делаете настоящую нейтрализацию настоящего вируса?
Козловская: Да, по классике… Мы сейчас работаем с несколькими базами, включая Коммунарку и еще несколько больниц, и получаем образцы от пациентов с нетипичным течением заболевания.
...
Гордейчук: Об этом мало говорят, но мы являемся единственным поставщиком Всемирной организации здравоохранения. 50% нашей продукции идет на экспорт. И 50% поставок вакцины желтой лихорадки в мире для ЮНИСЕФ производится у нас.
...
— Ваши иностранные «конкуренты» — китайские вакцины «Синовак», «Синофарм», индийская «Бхарат» — удивительно похожи на «КовиВак». Чем отличаются друг от друга инактивированные вакцины от коронавируса ?
Козловская: Мы все используем разные штаммы. Это, наверное, главное. Немного отличаются детали технологии инактивации и количество бета-пропиолактона.
— Значит ли это, что протективная эффективность «КовиВака» будет такая же, как в среднем у аналогов?
Козловская: «Синовак» и «Синофарм» ближе к китайскому штамму, в их штаммах нет, например, мутации D614G. Соответственно, возможно, у нас есть различия, может, у нас будут какие-то другие результаты, я не знаю, какая-то более длительная устойчивость к хранению или еще к чему-нибудь. Но ожидать большего результата, чем у них, было бы, мне кажется, с нашей стороны самонадеянно.
Кордубан: Вы поймите, мы изначально категорические пятерочники. Мы привыкли делать вакцины для детей, и для нас любая реакция на нашу вакцину — это кошмар, ужас, чьи-то слезы и все такое. Мы не только научно-исследовательский институт, мы еще и производство; соответственно, весь фармаконадзор мы ведем самостоятельно. Всю Сибирь, особенно детский контингент, на протяжении 40 лет прививаем ежегодно от клещевого энцефалита; 80% детей, покусанных собаками, лисами, ежами и так далее, попадают к нам за нашей инактивированной вакциной от бешенства. Поэтому мы понимаем, что у нас будет шквал звонков.
...
...Поэтому, когда мы исходно проверяли на мармозетках безопасность, а после — иммуногенность, — лично у меня уже не было вопросов по поводу того, что иммуногенность будет. Конечно, у всех людей, которые занимаются доклиническими исследованиями, есть любимая поговорка: мыши врут, а обезьяны преувеличивают. Но тем не менее у всех животных был [достаточный] уровень нейтрализующих антител.
...
— Вопрос, который я давно хочу задать. Бета-пропиолактон, инактивация, вирус… Два разных конформационных положения S-белка. Смотрели ли вы инактивированный вирус в электронный микроскоп? Что вы знаете про потерю S-белком своей части после инактивации? И не кажется ли вам, что это может быть для вас проблемой?
Инактивация вируса химическими веществами может приводить к тому, что в результате такой процедуры вирус «портится» — теряет часть белков, которые имеют значение для последующей выработки нейтрализующих антител. Риск такого развития событий в случае коронавируса связан с тем, что определенная часть его S-белка (который как раз очень важен для появления нейтрализующих антител) может быть непрочно соединена с остальной вирусной частицей в результате разрезания его ферментами. То, что ?-пропиолактон действительно может провоцировать потерю этой части, было показано в специальной работе оксфордских исследователей. Внешне такое действие инактивирующего вещества проявляется в изменении внешнего вида вирусных частиц под микроскопом: они теряют свои шипы — или, как говорят разработчики, «лысеют».
Гордейчук: Мы, конечно, посмотрели все в электронной микроскопии, посмотрели, что шипы все на месте и так далее, но на самом деле важнее все-таки функциональный тест. Мы каждой серией вакцины перед ее выходом в гражданский оборот иммунизируем мышей, и у них каждый раз есть нейтрализация.
...
Козловская: Так получилось, что в наши клинические исследования попали люди с уже имеющимся титром антител.
— Переболевшие или привитые?
Козловская: Переболевшие.
Кордубан: У них очень хорошая сероконверсия, антитела подрастают и не снижаются. Эмпирическим путем мы предполагаем, что ревакцинация будет точно такая же, как от гриппа, — ежегодно.
Гордейчук: Но она определенно будет по эпидпоказаниям, а не по антителам.
...
Антитела на любую перенесенную инфекцию, на вакцину, на что угодно, со временем будут снижаться. Мы знаем, что это коронавирусная инфекция — есть и другие коронавирусы, у них схожие белки, и антитела на них снижаются, скажем, быстрее, чем антитела на желтую лихорадку. Ну то есть это такой антиген, на который уровень антител снижается, и если мы получаем дико растянутую, лет на пять, кампанию по вакцинации, мы искусственно обогащаем вирус вариантами. Те, кто прививают от полиомиелита, прекрасно знают, что в национальные дни вакцинации в Индии делают по 200 миллионов прививок в сутки [чтобы такого не допустить].

«Когда привили первых добровольцев, тут все научились молиться» В России начали вакцинировать людей «КовиВаком» — а значит, пришла пора поговорить с его разработчиками. И мы это сделали — Meduza
В июне в России начали прививать третьей зарегистрированной в стране вакциной от ковида — «КовиВаком» производства Центра им. М. П. Чумакова. Эта вакцина сделана по самой старой, классической для такого рода препаратов технологии — и представляет собой инактивированный («убитый») вирус-возбудитель с добавкой стимулятора иммунитета. Найти вакцину пока непросто, но производители обещают, что уже в июне в гражданский оборот поступит миллион доз, а до конца года — пять-шесть миллионов. Журналисты «Медузы» Светлана Рейтер и Александр Ершов задали главные вопросы о «КовиВаке» сотрудникам центра Чумакова: замдиректора по качеству и инновациям Александре Синюгиной, замдиректора по регуляторным вопросам Екатерине Кордубан, завотделением инновационных биотехнологических препаратов Илье Гордейчуку и завотделом актуальных и вновь возникающих инфекций с пандемическим потенциалом Любови Козловской. Почему «КовиВак» стал лишь третьей по счету вакциной? Чем она отличается от других вакцин? Можем ли мы быть уверены, что вирус в вакцине действительно «убит» и не повредит нам? И почему разработчики считают, что обязательная вакцинация — это адекватная идея? // meduza.io...
Когда мы занимаемся разработкой вакцин, то пытаемся сделать эффективный и безопасный препарат — без оглядки на то, что сделали наши коллеги. Более того, мы полагаем, что в результате, когда пройдет какое-то время, возможно, самым оптимальным вариантом будет использовать разные модальности для ревакцинации.
На мой взгляд, вопрос о конкурентной бизнес-модели, о том, что мы будем продавать нашу вакцину с такими-то параметрами, а значит, «Спутник» себя будет продавать вот таким образом, некорректен. Мы это не для денег делаем.
...
Козловская: Мы не знаем, что будет через полгода. Мы, например, не знаем, кому нужны ревакцинации, сколько их будет нужно. И вообще, можно ли считать людей, привитых год назад, привитыми до сих пор. Нам предстоит собрать еще миллионы эпидемиологических данных. И в какой-то момент каждая из вакцин либо займет собственную нишу и будет существовать в ней — получит преимущества для людей каких-то определенных категорий, для каких-то определенных ситуаций и так далее, — либо обе вакцины будут взаимозаменяемыми.
...
— А сколько уже людей участвуют в исследованиях третьей фазы?
Синюгина: Исследования еще не начаты. У нас сейчас одобрено 18 клинических баз [лечебных учреждений], на три клинические базы мы ждем одобрения. Как только получим, начнем набор добровольцев…
— И там, в клиническом исследовании, половина доз — это плацебо?
Синюгина: Нет. Это неэтично с точки зрения эпидемиологической ситуации в России. Поэтому это открытое исследование без плацебо.
— Как определяется протективная эффективность препарата в исследованиях без плацебо?
Козловская: На сравнении с идентичной группой непривитых людей их популяции.
Синюгина: Мы прекрасно понимаем, что сейчас проводить плацебо-контролируемые исследования такого объема неэтично.
— Расскажите про вторую фазу исследований — про иммуногенность. Какие результаты вы получили, когда будет по ним информация? И когда будет [научная] статья по итогам второй фазы?
Козловская: Статья по доклиническим исследованиям отправлена на рецензию в один из ведущих зарубежных журналов.
...
Кордубан: У нас прошла первая фаза [исследований] — безопасность. Мы доказали свою безопасность. Дальше у нас идет вторая фаза — иммуногенность. Она проходила поэтапно: 200 человек в одной части, еще 200 — в другой. Финальный отчет, обработанный статистиками, мы должны получить в конце недели.
— А в вашем штамме, конечно, уханьский вирус?
Козловская: Нет. У нас европейский вариант с мутацией, D614G.
— Это подводит меня к вопросу: эффективна ли ваша вакцина против штамма дельта?
Козловская: Если бы он у меня был, если бы мне его кто-нибудь подарил… Нам пришлось, как и в первый раз, выделять его от больных, а в это время…
— В Институте Гамалеи вакцину проверяли на этом штамме, но с вами не поделились?
Козловская: Нет. Мы сейчас проверяем нашу вакцину на штамм дельта по смывам, которые получаем из больниц.
— А вы делаете настоящую нейтрализацию настоящего вируса?
Козловская: Да, по классике… Мы сейчас работаем с несколькими базами, включая Коммунарку и еще несколько больниц, и получаем образцы от пациентов с нетипичным течением заболевания.
...
Гордейчук: Об этом мало говорят, но мы являемся единственным поставщиком Всемирной организации здравоохранения. 50% нашей продукции идет на экспорт. И 50% поставок вакцины желтой лихорадки в мире для ЮНИСЕФ производится у нас.
...
— Ваши иностранные «конкуренты» — китайские вакцины «Синовак», «Синофарм», индийская «Бхарат» — удивительно похожи на «КовиВак». Чем отличаются друг от друга инактивированные вакцины от коронавируса ?
Козловская: Мы все используем разные штаммы. Это, наверное, главное. Немного отличаются детали технологии инактивации и количество бета-пропиолактона.
— Значит ли это, что протективная эффективность «КовиВака» будет такая же, как в среднем у аналогов?
Козловская: «Синовак» и «Синофарм» ближе к китайскому штамму, в их штаммах нет, например, мутации D614G. Соответственно, возможно, у нас есть различия, может, у нас будут какие-то другие результаты, я не знаю, какая-то более длительная устойчивость к хранению или еще к чему-нибудь. Но ожидать большего результата, чем у них, было бы, мне кажется, с нашей стороны самонадеянно.
Кордубан: Вы поймите, мы изначально категорические пятерочники. Мы привыкли делать вакцины для детей, и для нас любая реакция на нашу вакцину — это кошмар, ужас, чьи-то слезы и все такое. Мы не только научно-исследовательский институт, мы еще и производство; соответственно, весь фармаконадзор мы ведем самостоятельно. Всю Сибирь, особенно детский контингент, на протяжении 40 лет прививаем ежегодно от клещевого энцефалита; 80% детей, покусанных собаками, лисами, ежами и так далее, попадают к нам за нашей инактивированной вакциной от бешенства. Поэтому мы понимаем, что у нас будет шквал звонков.
...
...Поэтому, когда мы исходно проверяли на мармозетках безопасность, а после — иммуногенность, — лично у меня уже не было вопросов по поводу того, что иммуногенность будет. Конечно, у всех людей, которые занимаются доклиническими исследованиями, есть любимая поговорка: мыши врут, а обезьяны преувеличивают. Но тем не менее у всех животных был [достаточный] уровень нейтрализующих антител.
...
— Вопрос, который я давно хочу задать. Бета-пропиолактон, инактивация, вирус… Два разных конформационных положения S-белка. Смотрели ли вы инактивированный вирус в электронный микроскоп? Что вы знаете про потерю S-белком своей части после инактивации? И не кажется ли вам, что это может быть для вас проблемой?
Инактивация вируса химическими веществами может приводить к тому, что в результате такой процедуры вирус «портится» — теряет часть белков, которые имеют значение для последующей выработки нейтрализующих антител. Риск такого развития событий в случае коронавируса связан с тем, что определенная часть его S-белка (который как раз очень важен для появления нейтрализующих антител) может быть непрочно соединена с остальной вирусной частицей в результате разрезания его ферментами. То, что ?-пропиолактон действительно может провоцировать потерю этой части, было показано в специальной работе оксфордских исследователей. Внешне такое действие инактивирующего вещества проявляется в изменении внешнего вида вирусных частиц под микроскопом: они теряют свои шипы — или, как говорят разработчики, «лысеют».
Гордейчук: Мы, конечно, посмотрели все в электронной микроскопии, посмотрели, что шипы все на месте и так далее, но на самом деле важнее все-таки функциональный тест. Мы каждой серией вакцины перед ее выходом в гражданский оборот иммунизируем мышей, и у них каждый раз есть нейтрализация.
...
Козловская: Так получилось, что в наши клинические исследования попали люди с уже имеющимся титром антител.
— Переболевшие или привитые?
Козловская: Переболевшие.
Кордубан: У них очень хорошая сероконверсия, антитела подрастают и не снижаются. Эмпирическим путем мы предполагаем, что ревакцинация будет точно такая же, как от гриппа, — ежегодно.
Гордейчук: Но она определенно будет по эпидпоказаниям, а не по антителам.
...
Антитела на любую перенесенную инфекцию, на вакцину, на что угодно, со временем будут снижаться. Мы знаем, что это коронавирусная инфекция — есть и другие коронавирусы, у них схожие белки, и антитела на них снижаются, скажем, быстрее, чем антитела на желтую лихорадку. Ну то есть это такой антиген, на который уровень антител снижается, и если мы получаем дико растянутую, лет на пять, кампанию по вакцинации, мы искусственно обогащаем вирус вариантами. Те, кто прививают от полиомиелита, прекрасно знают, что в национальные дни вакцинации в Индии делают по 200 миллионов прививок в сутки [чтобы такого не допустить].



«Стало больше разрывов легких» Новые штаммы коронавируса несут еще более опасные симптомы. Чего от них ждать?
Как прогнозируют врачи, осенью в России ожидается очередной всплеск коронавируса. К чему готовиться россиянам, чем волны ковида отличаются друг от друга, появилось ли новое эффективное лечение — «Ленте.ру» рассказала инфекционист Первого Санкт-Петербургского медуниверситета им. Павлова Оксана Станевич. // lenta.ruСреди госпитализированных были вакцинированные пациенты?
Их было примерно 15 процентов. Но большинство из них не успели обрести иммунитет из-за того, что еще не прошло более двух недель после вакцинации. Какое-то количество пациентов было со сроками вакцинации старше четырех месяцев.
Были и привитые двумя дозами вакцины, получившие иммунитет. Но последние переносили инфекцию более-менее легко, никто из них не умер.
Вы говорите, что прививка для таких больных — один из способов противостоять длительному ковиду. Но эффективность вакцинации у иммуноскомпрометированных низкая. Может ли она вообще быть нулевой?
В других странах проводятся исследования, которые анализируют, какие конкретно группы пациентов, в зависимости от диагноза и типа лечения, хуже отвечают на вакцину. Нельзя сказать, что все эти пациенты вообще не отвечают на вакцинацию, если она проведена в надлежащие сроки. Для онкологических больных — это до начала противоопухолевой терапии или в промежутках между ее циклами.
В настоящее время я пытаюсь инициировать исследование о вакцинации именно таких пациентов. Планируется изучение их иммунного ответа, его длительности в зависимости от видов терапии. Это работа как раз поможет оценить, работает ли вакцинация у таких пациентов не только в предотвращении тяжелого заболевания ковидом и смерти, но и в предотвращении длительного вирусовыделения. Пока мы находимся на этапе поиска спонсора: для такого исследования необходимо финансирование.


Было в радионовостях, что ланцет тиснул статейку о длительности действия вакцин.
Основная мысль, что эффективность вакцинирования ослабевает за 6 месяцев не благодаря появлению новых штаммов, а сама по себе. И численно величина защиты составляет порядка 40% от первоначальной.
Кто на ланцете ориентируется, оригинал встречали?
Основная мысль, что эффективность вакцинирования ослабевает за 6 месяцев не благодаря появлению новых штаммов, а сама по себе. И численно величина защиты составляет порядка 40% от первоначальной.
Кто на ланцете ориентируется, оригинал встречали?

Для тех, кого забанили в гугле, вероятно вот эта

Одним словом - падает для всех почти одинаково

Effectiveness of mRNA BNT162b2 COVID-19 vaccine up to 6 months in a large integrated health system in the USA: a retrospective cohort study
Our results provide support for high effectiveness of BNT162b2 against hospital admissions up until around 6 months after being fully vaccinated, even in the face of widespread dissemination of the delta variant. Reduction in vaccine effectiveness against SARS-CoV-2 infections over time is probably primarily due to waning immunity with time rather than the delta variant escaping vaccine protection. // www.thelancet.comOverall vaccine effectiveness against infection with the delta variant for the fully vaccinated was 75% (95% CI 71–78), while overall vaccine effectiveness for other variants was 91% (88–92; appendix pp 9–10). Estimates against both delta and other variants were high within 1 month after full vaccination (vaccine effectiveness against delta 93% [95% CI 85–97] vs other variants 97% [95–99]; p=0·29). At 4 months after full vaccination, vaccine effectiveness against delta infections declined
to 53% (95% CI 39–65) and vaccine effectiveness against other variants declined to 67% (45–80; p=0·25). The difference in rate of decline in vaccine effectiveness between delta and other variants was not significant (p=0·30). For specimens in which a sequence could not be determined, adjusted vaccine effectiveness after full vaccination declined from 84% [95% CI 78–88]) at less than 1 month to 47% (30–59) after 4 months (figure 3;appendix pp 10–11). Among the fully vaccinated, vaccine effectiveness against hospital admissions was 93% (95% CI 84–96) for delta and 95% (90–98) for other
variants. Effectiveness against hospital admissions waslower among specimens that failed sequencing (vaccine effectiveness 77% [95% CI 67–85]; appendix pp 10–11).
Одним словом - падает для всех почти одинаково


Статья старая, но оставлю здесь
[round_box]
The world has bet the farm on vaccines as the solution to the pandemic, but the trials are not focused on answering the questions many might assume they are. Peter Doshi reports As phase III trials of covid-19 vaccines reach their target enrolments, officials have been trying to project calm. The US coronavirus czar Anthony Fauci and the Food and Drug Administration leadership have offered public assurances that established procedures will be followed.1234 Only a “safe and effective” vaccine will be approved, they say, and nine vaccine manufacturers issued a rare joint statement pledging not to prematurely seek regulatory review.5 But what will it mean exactly when a vaccine is declared “effective”? To the public this seems fairly obvious. “The primary goal of a covid-19 vaccine is to keep people from getting very sick and dying,” a National Public Radio broadcast said bluntly.6 Peter Hotez, dean of the National School of Tropical Medicine at Baylor College of Medicine in Houston, said, “Ideally, you want an antiviral vaccine to do two things . . . first, reduce the likelihood you will get severely ill and go to the hospital, and two, prevent infection and therefore interrupt disease transmission.”7 Yet the current phase III trials are not actually set up to prove either (table 1). None of the trials currently under way are designed to detect a reduction in any serious outcome such as hospital admissions, use of intensive care, or deaths. Nor are the vaccines being studied to determine whether they can interrupt transmission of the virus. View this table: Table 1 Characteristics of ongoing phase III covid-19 vaccine trials In a September interview Medscape editor in chief Eric Topol pondered what counts as a recorded “event” in the vaccine trials. “We’re not talking about just a PCR [polymerase …
// www.bmj.com [/round_box]
Ну собственно случай в клинике в Израиле, описанный в научной статье, это наглядно и показал...
[round_box]

Will covid-19 vaccines save lives? Current trials aren’t designed to tell us
The world has bet the farm on vaccines as the solution to the pandemic, but the trials are not focused on answering the questions many might assume they are. Peter Doshi reports As phase III trials of covid-19 vaccines reach their target enrolments, officials have been trying to project calm. The US coronavirus czar Anthony Fauci and the Food and Drug Administration leadership have offered public assurances that established procedures will be followed.1234 Only a “safe and effective” vaccine will be approved, they say, and nine vaccine manufacturers issued a rare joint statement pledging not to prematurely seek regulatory review.5 But what will it mean exactly when a vaccine is declared “effective”? To the public this seems fairly obvious. “The primary goal of a covid-19 vaccine is to keep people from getting very sick and dying,” a National Public Radio broadcast said bluntly.6 Peter Hotez, dean of the National School of Tropical Medicine at Baylor College of Medicine in Houston, said, “Ideally, you want an antiviral vaccine to do two things . . . first, reduce the likelihood you will get severely ill and go to the hospital, and two, prevent infection and therefore interrupt disease transmission.”7 Yet the current phase III trials are not actually set up to prove either (table 1). None of the trials currently under way are designed to detect a reduction in any serious outcome such as hospital admissions, use of intensive care, or deaths. Nor are the vaccines being studied to determine whether they can interrupt transmission of the virus. View this table: Table 1 Characteristics of ongoing phase III covid-19 vaccine trials In a September interview Medscape editor in chief Eric Topol pondered what counts as a recorded “event” in the vaccine trials. “We’re not talking about just a PCR [polymerase …
// www.bmj.com [/round_box]
But what will it mean exactly when a vaccine is declared “effective”? To the public this seems fairly obvious. “The primary goal of a covid-19 vaccine is to keep people from getting very sick and dying,” a National Public Radio broadcast said bluntly.6
Peter Hotez, dean of the National School of Tropical Medicine at Baylor College of Medicine in Houston, said, “Ideally, you want an antiviral vaccine to do two things . . . first, reduce the likelihood you will get severely ill and go to the hospital, and two, prevent infection and therefore interrupt disease transmission.”
Yet the current phase III trials are not actually set up to prove either (table 1). None of the trials currently under way are designed to detect a reduction in any serious outcome such as hospital admissions, use of intensive care, or deaths. Nor are the vaccines being studied to determine whether they can interrupt transmission of the virus.
Но что в действительности означает, когда вакцину называют "эффективной" ? Для обывателя ответ представляется очевидным. "Изначальная цель вакцин против ковид-19 состоит в том, чтобы защитить людей от тяжелой болезни и смерти" - прямо заявляют национальные СМИ.
Питер Хотес, декан национальной школы тропической медицины в колледже медицны Бейлора в Хьюстоне сказал: "В идеале вы хотите чтобы антивирусная вакцина делала две вещи... во-1 сокращала вероятность того, что вы заболеете тяжело и будете госпитализированы и во-2 предотвращала инфицирование и тем самым прерывала распространение инфекции.
Тем не менее, текущая фаза III испытаний вовсе не предназначена для того чтобы доказать эти обе вещи.
Ни одно из испытаний которые сейчас идут, не сконструированы таким образом, чтобы обнаружить сокращение тяжелых случаев, требующих госпитализации, использовании интенсивной терапии или смерти. Ни одна из вакцин, которые сейчас разрабатываются, не исследуется на предмет предотвращения распространения инфекции
Ну собственно случай в клинике в Израиле, описанный в научной статье, это наглядно и показал...


Спасибо, но таки в посту справа указано, с чего пишется. В моем случае телефон. Гуглить неудобно.


Fakir:
предупреждение (+1) по категории «Флуд или офтопик»
На телефоны уже стали ставить Линукс ??? 

Прикреплённые файлы:


Fakir:
предупреждение (+1) по категории «Флуд или офтопик»

AstraZeneca назвала эффективность своего коктейля от COVID-19
Компания заявила, что разработала первый в мире комбинированный препарат, который работает и как лечение, и как профилактика COVID-19. Исследования показали, что он на 50–67% снижает риск тяжелого течения и смерти от этой инфекции // www.rbc.ruФармацевтическая компания AstraZeneca сообщила, что последняя стадия исследования ее нового лекарства от COVID-19 на основе антител свидетельствует о его эффективности, сообщение опубликовано на ее сайте.
Лекарство представляет собой коктейль на основе двух видов антител и получило название AZD7442. Оно на 50% снижает риск тяжелого течения болезни или смерти пациентов, которые не были госпитализированы, если симптомы перед получением AZD7442 у них держались в течение недели. В случае если человек заболел менее пяти дней перед началом приема, риск перенести болезнь тяжело или умереть снижается на 67%. Препарат вводится инъекцией внутримышечно. Защита, которую он дает организму, может длиться более шести месяцев.
Это первое лекарство от коронавируса, которое работает как профилактика против заражения и как лекарство от болезни, уточняют в компании. Оно было разработано, чтобы защитить людей, у которых недостаточно силен иммунный ответ на вакцины.
Окончательные результаты исследования AstraZeneca обещала опубликовать позже.


С Чумаковской вакциной смешно получилось...
А если бы "не совсем инактивированная партия" попала бы не в те волосатые руки
А если бы "не совсем инактивированная партия" попала бы не в те волосатые руки


yacc> Для тех, кого забанили в гугле, вероятно вот эта
yacc> Effectiveness of mRNA BNT162b2 COVID-19 vaccine up to 6 months in a large integrated health system in the USA: a retrospective cohort study - The Lancet
Если перевести статью из процентов в разы, получится более наглядно:
Вакцина в среднем снижает шансы заразиться "дельтой" в 4 раза, другими штаммами в 11 раз (за срок исследования).
При этом через 1 месяц после полной вакцинации: дельтой в 14.3 раза, другими штаммами в 33 раза.
Через 4 месяца: дельтой в 2 раза, другими штаммами в 3 раза.
Для полностью вакцинированных шансы попасть в госпиталь с дельтой уменьшаются в среднем в 14.3 раза, с другими штаммами в 20 раз.
Там еще про эффективность у тех, кто нарушил порядок/сроки прививок. Но я не стал переводить этот кусок.
Когда смотришь на результаты в разах, то видно чудовищно быстрое падение эффективности. Увы и ах.
Для того, чтоб эпидемия затухла нужно чтоб эффект от вакцины "в разах" был больше коэффициента R0. R0 у дельты с нынешним стилем жизни оценивали примерно в 4.
Это значит, что не просто вирус с нами навсегда. Но и сама пандемия с нами очень надолго.
Т.е. мы к ней привыкнем. Уже почти привыкли. И будем лишь бороться за уменьшение смертности. Как сведем смертность к "гриппозным" 0.7% так и успокоимся.
Лет еще через 10 разработаем эффективные экспресс тесты. Вакцина станет обязательной, как сейчас от дифтерии. И снова можно будет ездить по миру. А для поездок в неблагополучные регионы - полна жопа уколов. Как в 50-е, 60-е годы.
Есть конечно шанс, что мы все переболеем и получим естественный иммунитет. Но на это надеяться не нужно. Вирус может, и будет мутировать быстрее, чем человечество приобретает иммунитет.
yacc> Effectiveness of mRNA BNT162b2 COVID-19 vaccine up to 6 months in a large integrated health system in the USA: a retrospective cohort study - The Lancet
Если перевести статью из процентов в разы, получится более наглядно:
Вакцина в среднем снижает шансы заразиться "дельтой" в 4 раза, другими штаммами в 11 раз (за срок исследования).
При этом через 1 месяц после полной вакцинации: дельтой в 14.3 раза, другими штаммами в 33 раза.
Через 4 месяца: дельтой в 2 раза, другими штаммами в 3 раза.
Для полностью вакцинированных шансы попасть в госпиталь с дельтой уменьшаются в среднем в 14.3 раза, с другими штаммами в 20 раз.
Там еще про эффективность у тех, кто нарушил порядок/сроки прививок. Но я не стал переводить этот кусок.
Когда смотришь на результаты в разах, то видно чудовищно быстрое падение эффективности. Увы и ах.
Для того, чтоб эпидемия затухла нужно чтоб эффект от вакцины "в разах" был больше коэффициента R0. R0 у дельты с нынешним стилем жизни оценивали примерно в 4.
Это значит, что не просто вирус с нами навсегда. Но и сама пандемия с нами очень надолго.
Т.е. мы к ней привыкнем. Уже почти привыкли. И будем лишь бороться за уменьшение смертности. Как сведем смертность к "гриппозным" 0.7% так и успокоимся.
Лет еще через 10 разработаем эффективные экспресс тесты. Вакцина станет обязательной, как сейчас от дифтерии. И снова можно будет ездить по миру. А для поездок в неблагополучные регионы - полна жопа уколов. Как в 50-е, 60-е годы.
Есть конечно шанс, что мы все переболеем и получим естественный иммунитет. Но на это надеяться не нужно. Вирус может, и будет мутировать быстрее, чем человечество приобретает иммунитет.


kot1967>> С Чумаковской вакциной смешно получилось...
kot1967>> А если бы "не совсем инактивированная партия" попала бы не в те волосатые руки
Invar> Эээ... а подробности?
Invar> Про внезапну© модернизацию производства новости на слуху
Ну типа вкололи "Ковиваку" хорошему человеку из Минздрава а тот "бац" и заболел понимаешь... или вообще крякнул не суть... начали разбираться ну и типа получилось что типа вкололи живой вирус "хорошему человеку". А поскольку человек был очень хороший то на тормозах спустить не удалось завернули "партию". Ну это все так типа типа "вы все врете", как там на самом деле было - хз
kot1967>> А если бы "не совсем инактивированная партия" попала бы не в те волосатые руки
Invar> Эээ... а подробности?
Invar> Про внезапну© модернизацию производства новости на слуху
Ну типа вкололи "Ковиваку" хорошему человеку из Минздрава а тот "бац" и заболел понимаешь... или вообще крякнул не суть... начали разбираться ну и типа получилось что типа вкололи живой вирус "хорошему человеку". А поскольку человек был очень хороший то на тормозах спустить не удалось завернули "партию". Ну это все так типа типа "вы все врете", как там на самом деле было - хз


Invar>>> Про внезапну© модернизацию производства новости на слуху
kot1967>> Ну типа вкололи "Ковиваку" хорошему человеку из Минздрава...
Invar> Чтот-то вроде с полгода назад пробегалло
Invar> А чем там кстати гря инактивируют? Не спиртом?


По ГОСТу спиртовую инактивацию проводит сам пациент уже непосредственно после введение вакцины, перорально по возможности.. ..
kot1967>> Ну типа вкололи "Ковиваку" хорошему человеку из Минздрава...
Invar> Чтот-то вроде с полгода назад пробегалло
Invar> А чем там кстати гря инактивируют? Не спиртом?



По ГОСТу спиртовую инактивацию проводит сам пациент уже непосредственно после введение вакцины, перорально по возможности.. ..


Fakir:
предупреждение (+1) по категории «Флуд или офтопик»
- Fakir [17.10.2021 16:37]: Предупреждение пользователю: kot1967#17.10.21 12:11
- Fakir [17.10.2021 23:08]: Предупреждение пользователю: yacc#08.10.21 19:49
- Fakir [17.10.2021 23:08]: Предупреждение пользователю: Bredonosec#08.10.21 16:29
Copyright © Balancer 1997..2024
Создано 13.11.2013
Связь с владельцами и администрацией сайта: anonisimov@gmail.com, rwasp1957@yandex.ru и admin@balancer.ru.
Создано 13.11.2013
Связь с владельцами и администрацией сайта: anonisimov@gmail.com, rwasp1957@yandex.ru и admin@balancer.ru.
 Invar
Invar

 инфо
инфо инструменты
инструменты Bredonosec
Bredonosec

 кщееш
кщееш

 Invar
Invar


 Fakir
Fakir




 Invar
Invar

 Invar
Invar
